午后,基因研究中心接到一份结肠癌患者的组织样本,家属急切地询问:“医生,听说可以做一个叫MSI的检测,能指导用药?这到底是什么,怎么做出来的?” 这样的场景在中心的咨询室几乎每天都会上演。在精准医疗时代,微卫星不稳定性(MSI) 已成为指导多种实体瘤(尤其是结直肠癌、子宫内膜癌)免疫治疗和预后评估的关键生物标志物。它的检测流程,远非“做个化验”那么简单,背后是一整套严谨、精细的科学操作。
MSI检测,到底是在检测什么?
简单来说,我们是在检测肿瘤细胞DNA的“复制品控”是否失灵。您可以把微卫星想象成DNA链上一些非常短的、像“A-A-A-A”或“C-A-C-A-C-A”这样重复排列的序列,它们是基因组的“路标”。正常情况下,细胞复制DNA时,有专门的“纠错系统”(错配修复系统,MMR)来确保这些“路标”被精准复制。但当MMR系统功能缺失时,这些微卫星在复制过程中就容易出错,长度发生改变——这就叫“微卫星不稳定”。
医生说要取肿瘤组织,取哪里才对?
这是流程的起点,也是关键。检测需要两类样本:肿瘤组织和正常对照组织。肿瘤组织通常来自手术切除或活检的病理蜡块。而正常对照,最理想的是同一患者的血液、唾液,或者远离肿瘤的正常组织(如癌旁组织)。核心原则是:对照组织的DNA必须能代表患者与生俱来的、未受肿瘤影响的“原始基因蓝图”。如果只拿肿瘤组织,我们无从判断那些变化是肿瘤特有的,还是患者天生就有的。

从一块组织到DNA,中间经历了什么?
病理科医生会在显微镜下,从蜡块中小心地“圈出”富含肿瘤细胞的目标区域(这个过程叫“显微切割”),确保我们提取的DNA主要来自肿瘤细胞,避免被大量正常细胞“稀释”。接着,通过专业试剂盒,从这些圈定的细胞中提取出高质量的DNA。这一步听起来简单,但DNA的纯度和完整性直接决定了后续实验的成败。
实验室里,如何“看清”那些微小的序列变化?
这是技术的核心。目前的金标准方法是多重荧光PCR结合毛细管电泳。简单解释:我们设计好特异的“引物”(可以理解为精准的“探针”),去扩增肿瘤DNA和正常对照DNA中那几个公认的、最容易出问题的微卫星位点(通常为5个,如BAT-25, BAT-26等)。扩增后的产物,会带有荧光标记。
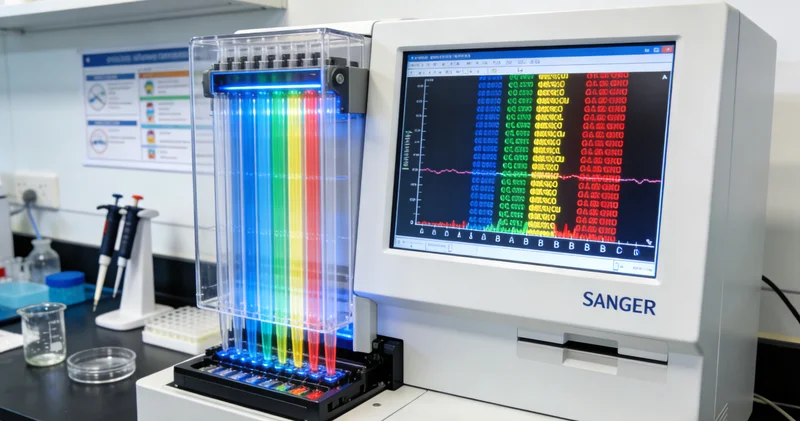
然后,让这些带荧光的DNA片段在毛细管中“赛跑”——片段越短,“跑”得越快。最后提一嘴,仪器会生成两张像山峰一样的图谱:一张来自肿瘤DNA,一张来自正常对照DNA。我们的眼睛(和软件)要做的,就是仔细比对这两张图谱上,同一个微卫星位点对应的“山峰”位置是否一致。
怎么看结果?什么叫“不稳定”?
比对图谱是决定性的一步。如果某个位点在肿瘤样本中出现了正常对照中没有的、位置偏移的“新山峰”(即片段长度发生了改变),这个位点就被判读为“不稳定”。根据国际共识,如果5个位点中有2个及以上不稳定,就判定为MSI-H(高频微卫星不稳定);1个不稳定为MSI-L(低频);0个不稳定则为MSS(微卫星稳定)。通常,只有MSI-H的状态才对临床决策具有明确的指导意义。
除了PCR,还有别的方法吗?
当然有。二代测序(NGS) 现在是越来越主流的方法。它不局限于那几个固定位点,可以一次性扫描成百上千个微卫星位点,信息量更大,也更适合与其它基因突变一同检测。此外,还有一种间接的方法:通过免疫组化(IHC)检测MMR系统相关蛋白(MLH1, MSH2, MSH6, PMS2)是否缺失。如果蛋白缺失,通常意味着MMR功能缺陷,也高度提示MSI-H状态。IHC法更快、成本更低,常被用作初筛。
报告出来了,上面的结果意味着什么?
一份完整的MSI检测报告,会明确给出MSI状态(MSI-H/MSI-L/MSS)。对于临床医生和患者而言,MSI-H是一个非常重要的“绿灯”信号。它强烈提示肿瘤对免疫检查点抑制剂(如PD-1/PD-L1抑制剂)治疗可能高度有效,因为这类型肿瘤突变多,更容易被免疫系统识别。同时,MSI-H也关联着特定的遗传综合征(林奇综合征)筛查和预后信息。拿到报告后,主治医生会结合肿瘤类型、分期等具体情况,为您解读并制定个体化的治疗方案。
从一块小小的组织,到一份影响治疗决策的报告,MSI检测之路凝聚了病理、检验、生物信息等多学科团队的协作。理解这个过程,或许能让您在面对那些专业术语时,多一份了然,也多一份与医生共同决策的底气。精准医疗,正始于对这些微观世界变化的精准洞察。
